Termodinamica dell'ingegneria chimica
Salve ragazzi chi.potrebbe aiutarmi?
Non riesco a risolvere alcuni esercizi (sto.preparando l'esame e sono.davvero in difficolta')
Questi sono gli esercizi estrapolati dal testo fondamenti dell'ingegneria chimica di Renato Rota:
1)si vuole alzare la temperatura di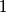
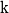
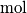 di anidride carbonica da
di anidride carbonica da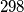
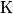 a
a 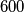
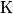 mantenendo la pressione costante.
mantenendo la pressione costante.
Calcolare la quantita' di calore da fornire. Si consideri il gas perfetto.
2 )un compressore aspira aria in quiete a
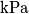 e
e 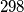
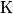 e la scarica a
e la scarica a 
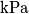 e
e 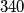
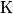 .
.
Assumendo la velocita' allo scarico pari a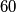
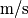 e che il compressore lavori adiabaticamente, calcolare la potenza richiesta per conprimere
e che il compressore lavori adiabaticamente, calcolare la potenza richiesta per conprimere 
 di aria.
di aria.
Si consideri l'aria un gas perfetto con un calore specifico a pressione costante pari a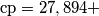
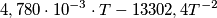 J/mol K
J/mol K
Non riesco a risolvere alcuni esercizi (sto.preparando l'esame e sono.davvero in difficolta')
Questi sono gli esercizi estrapolati dal testo fondamenti dell'ingegneria chimica di Renato Rota:
1)si vuole alzare la temperatura di
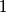
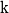
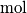 di anidride carbonica da
di anidride carbonica da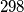
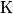 a
a 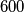
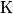 mantenendo la pressione costante.
mantenendo la pressione costante. Calcolare la quantita' di calore da fornire. Si consideri il gas perfetto.
2 )un compressore aspira aria in quiete a

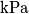 e
e 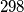
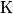 e la scarica a
e la scarica a 
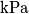 e
e 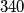
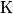 .
.Assumendo la velocita' allo scarico pari a
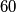
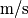 e che il compressore lavori adiabaticamente, calcolare la potenza richiesta per conprimere
e che il compressore lavori adiabaticamente, calcolare la potenza richiesta per conprimere 
 di aria.
di aria.Si consideri l'aria un gas perfetto con un calore specifico a pressione costante pari a
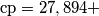
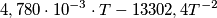 J/mol K
J/mol K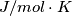
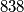
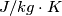
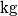 .
.