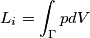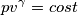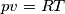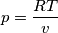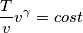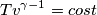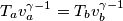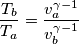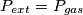Variazione dell'Entropia in un gas perfetto
Due moli di gas perfetto sono contenute in un cilindro termicamente isolante chiuso da un pistone di massa trascurabile. All'esterno del cilindro c'è il vuoto. Calcolare la variazione di entropia del gas quando si espande liberamente fino ad occupare un volume triplo di quello iniziale.
La formula che esprime la variazione dell'entropia dovrebbe essere questa:
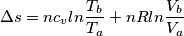
Il mio problema sta nel capire come ottenere il calore molare. In oltre, correggetemi se sbaglio, se il volume triplica, triplica pure la temperatura giusto?
La formula che esprime la variazione dell'entropia dovrebbe essere questa:
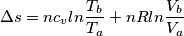
Il mio problema sta nel capire come ottenere il calore molare. In oltre, correggetemi se sbaglio, se il volume triplica, triplica pure la temperatura giusto?
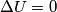
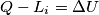 dove
dove 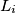 è il lavoro interno, che comprende il lavoro di espansione delle superfici del sistema
è il lavoro interno, che comprende il lavoro di espansione delle superfici del sistema