Termodinamica, II principio
Moderatori: ![]() IsidoroKZ,
IsidoroKZ, ![]() PietroBaima,
PietroBaima, ![]() Ianero
Ianero
0
voti
Quindi, per tenere in piedi tutto, dobbiamo considerare ogni sub-regione di qualsiasi dimensione all'interno di V contenente sufficienti elementi tali che la loro velocità media coincida con la T globale?
«Non tutto ciò che tecnicamente può essere fatto deve necessariamente essere fatto.»
R.L.M.
R.L.M.
-

 Fernecchio
Fernecchio
972 1 2 4 - Frequentatore

- Messaggi: 290
- Iscritto il: 14 ott 2012, 17:52
0
voti
dipende dal modello.
Un modello del genere fa delle previsioni corrette finché il volume delle molecole è trascurabile rispetto al dominio.
Un modello del genere fa delle previsioni corrette finché il volume delle molecole è trascurabile rispetto al dominio.
-

 PietroBaima
PietroBaima
90,7k 7 12 13 - G.Master EY

- Messaggi: 12207
- Iscritto il: 12 ago 2012, 1:20
- Località: Londra
0
voti
Fernecchio ha scritto:Quindi, per tenere in piedi tutto, dobbiamo considerare ogni sub-regione di qualsiasi dimensione all'interno di V contenente sufficienti elementi tali che la loro velocità media coincida con la T globale?
Sì, ma quella che tu metti come condizione, io la considererei un effetto.
Bisogna che il numero di molecole sia infinito per fare in modo che la distribuzione di velocità coincida con un singolo valore. Questa proprietà viene ereditata da qualsiasi partizione dell'insieme, provando il principio.
0
voti
In generale, un sistema tende ad evolvere verso lo "stato di equilibrio" (cioè verso lo "stato macroscopico" più probabile, cioè verso lo "stato macroscopico" associato al maggior numero di "stati microscopici", e quindi ad entropia maggiore).
Raggiunto questo, le molecole continuano a muoversi caoticamente, e quindi è probabile che si possano osservare delle fluttuazioni, cioè delle deviazioni dallo stato di equilibrio per un certo lasso di tempo, e maggiore è il numero delle molecole, minore è l' ampiezza che avranno queste fluttuazioni.
Prendo due esempi presi dai miei appunti:
consideriamo un gas perfetto in un contenitore adiabatico a pareti rigide, suddiviso in due parti uguali da un setto adiabatico fisso.
Supponiamo il gas inizialmente solo nella metà sinistra del contenitore.
Se rimuoviamo il setto, ciascuna molecola avrà la possibilità di occupare il doppio delle posizioni occupabili inizialmente, a setto inserito.
Quindi, togliendo il setto, l' entropia aumenta di un fattore:
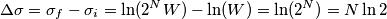 , dove N è il numero di molecole, e W è la probabilità termodinamica dello stato iniziale.
, dove N è il numero di molecole, e W è la probabilità termodinamica dello stato iniziale.
Se N è il numero di Avogadro, cioè il numero di particelle contenute in una mole di sostanza, si ha che il fattore 2^N è talmente elevato da poter considerare trascurabile la probabilità di osservare il processo inverso, cioè una compressione spontanea (credo che questo sia vero anche se il tempo di osservazione fosse confrontabile con quello della vita dell' intero Universo).
Un altro esempio: consideriamo due corpi a temperatura diversa a contatto.
Uno lo chiamiamo C (corpo caldo) e l' altro F (corpo freddo).
Il sistema tende ad evolvere verso lo "stato di equilibrio" , nel quale i due corpi hanno temperatura identica; quindi, C si troverà a dover cedere energia al corpo F.
In un sistema costituito da pochissimi atomi, ci potrà pure essere la possibilità di riuscire ad osservare (nell' arco della nostra vita) "fluttuazioni" (cioè deviazioni dallo stato di equilibrio) in cui per un certo lasso di tempo l' energia del corpo C aumenti a spese di quella del corpo F, ma in un sistema costituito da un numero di atomi confrontabile con il numero di Avogadro, questa possibilità è estremamente bassa.
Non nego che potrei aver scritto castronerie, inoltre ho usato termini come: "estremamente", "elevato", "trascurabile",ecc., che non piacciono a PietroBaima
PietroBaima  , ma non ho saputo far di meglio.
, ma non ho saputo far di meglio. 
Raggiunto questo, le molecole continuano a muoversi caoticamente, e quindi è probabile che si possano osservare delle fluttuazioni, cioè delle deviazioni dallo stato di equilibrio per un certo lasso di tempo, e maggiore è il numero delle molecole, minore è l' ampiezza che avranno queste fluttuazioni.
Prendo due esempi presi dai miei appunti:
consideriamo un gas perfetto in un contenitore adiabatico a pareti rigide, suddiviso in due parti uguali da un setto adiabatico fisso.
Supponiamo il gas inizialmente solo nella metà sinistra del contenitore.
Se rimuoviamo il setto, ciascuna molecola avrà la possibilità di occupare il doppio delle posizioni occupabili inizialmente, a setto inserito.
Quindi, togliendo il setto, l' entropia aumenta di un fattore:
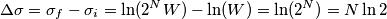 , dove N è il numero di molecole, e W è la probabilità termodinamica dello stato iniziale.
, dove N è il numero di molecole, e W è la probabilità termodinamica dello stato iniziale.Se N è il numero di Avogadro, cioè il numero di particelle contenute in una mole di sostanza, si ha che il fattore 2^N è talmente elevato da poter considerare trascurabile la probabilità di osservare il processo inverso, cioè una compressione spontanea (credo che questo sia vero anche se il tempo di osservazione fosse confrontabile con quello della vita dell' intero Universo).
Un altro esempio: consideriamo due corpi a temperatura diversa a contatto.
Uno lo chiamiamo C (corpo caldo) e l' altro F (corpo freddo).
Il sistema tende ad evolvere verso lo "stato di equilibrio" , nel quale i due corpi hanno temperatura identica; quindi, C si troverà a dover cedere energia al corpo F.
In un sistema costituito da pochissimi atomi, ci potrà pure essere la possibilità di riuscire ad osservare (nell' arco della nostra vita) "fluttuazioni" (cioè deviazioni dallo stato di equilibrio) in cui per un certo lasso di tempo l' energia del corpo C aumenti a spese di quella del corpo F, ma in un sistema costituito da un numero di atomi confrontabile con il numero di Avogadro, questa possibilità è estremamente bassa.
Non nego che potrei aver scritto castronerie, inoltre ho usato termini come: "estremamente", "elevato", "trascurabile",ecc., che non piacciono a

0
voti
Ok, confermo che è qua che non ci capiamo. Provo a riproporti cosa c'è che non va.angel99 ha scritto:Non credo sia questo, sai? E' un po' più sottile. Se rileggi dall'inizio, non ho mai citato temperature locali, zone calde o fredde, o cose similari. La temperatura è sempre quella media, perché si riferisce a una massa di gas.
Tu dici: ho un contenitore adiabatico con dentro un gas alla temperatura T. Facciamo un esempio, prendendo numeri proprio a caso e per cui sia facile fare dei conti. Facciamo che la temperatura media del gas è
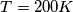 . perché dico media? Beh penso che siamo d'accordo che di totalmente uniforme nel mondo ci sia poco.
. perché dico media? Beh penso che siamo d'accordo che di totalmente uniforme nel mondo ci sia poco. Se proprio vogliamo fare i precisi allora aggiungiamo nello spazio dopo media ( e anche dopo uniforme, volendo).
Bene. Ora tu (non tu in realtà, vabbè ci siamo capiti
Spariamo qualche altro numero a caso. Supponiamo che la velocità media delle molecole sia quanto?
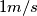 facciamo. Pertanto, a 1 m/s corrisponde una temperatura di 200K.
facciamo. Pertanto, a 1 m/s corrisponde una temperatura di 200K. Ora, veniamo al punto in cui non ci intendiamo.
Prendi un contenitore, che ne so di plastica. Mettilo su una fiamma ossidrica. Sto esempio fa schifo ma al momento non mi veniva nulla di meglio. Cosa succede? la fiamma scalda l'aria dentro il contenitore. Dove principalmente? Dove ci ho messo la fiamma. Bene. Qual è la temperatura media (nello spazio) del gas? Boh, 300K. Qual è la temperatura del gas della regione che sta vicino alla fiamma ossidrica? Beh ho fornito energia scaldando con la fiamma, le molecole si muovono di più, ho una temperatura di faciamo 400. alla parte opposta del contenitore? 200. Media? 300. Detta così alla buona. In realtà dovresti fare la media integrale delle temperature in ogni elementino di spazio dV e otterresti 300K. Anche fino a qua penso che siamo d'accordo. DOMANDA: E' corretto dire che il gas ha temperatura 300K? Io direi di no. Io direi ce c'è una parte di gas a tempratura di 400, l'altra di 200. Poi, per carità, la temperatura media è 300. Ma se tocco dalla parte del contenitore dove ci sono i 400 mi scotto, se tocco dall'altra no.
Ora, cosa dici tu?
Consideriamo ora un setto divisorio mobile, adiabatico S che possa partizionare il contenitore in due volumi uguali V1 e V2.
Bene
Azioniamo tale setto separando il gas in due ambienti distinti. In ciascuno dei due volumi avremo gas alla medesima temperatura perché avremo separato un numero eguale di atomi con eguale velocità media.
Vero, solo se la velocità media (quadratica) E' UGUALE IN TUTTO LO SPAZIO, cioè quasi mai, infatti, come dici tu :
Ma questo è solo mediamente vero!
Anzi, a meno di una probabilità infinitesima, azionando il setto posso essere certo di aver suddiviso due gruppi di atomi con velocità medie (e quindi temperature) diverse!
Bene. Prima del setto, le due temperature erano già diverse di loro. Il setto, come ho scritto in un altro post, non fa nulla, separa due regioni a temperature di per loro diverse.
L'errore sta qua
partire da (V, T) giungendo a (V/2, T1) + (V/2, T2) con T1 > T2
Tu consideri la temperatura media del gas T come se fosse costante in tutto lo spazio. Così non è. perché appunto, se in una certa regione, per quanto piccola e in un certo istante, hai una velocità media di 3 mentre in un'altra ha una velocità media di 2 nella prima hai 300K, nella seconda 400. Tu da una parte pretendi che la temperatura sia costante in tutto il volume, dall'altra che ci siano delle zone in cui in certi istanti nel tuo volume in cui le particelle vanno più veloci delle particelle in un'altra regione. Questa è una contraddizione Non fai lavoro, non CREI nulla. La citazione andrebbe scritta parti da (V1,T1)+(V2,T2) arrivi........................ con la stessa roba. Ci hai solo messo un qualcosa in mezzo.
Quello che sostengo io è la stessa cosa detta nel post precedente da
Chi c’è in linea
Visitano il forum: Nessuno e 13 ospiti

 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra) pigreco]=π
pigreco]=π