Deriva degli elettroni
Moderatori: ![]() carloc,
carloc, ![]() g.schgor,
g.schgor, ![]() BrunoValente,
BrunoValente, ![]() IsidoroKZ
IsidoroKZ
0
voti
A quanto ho capito da google, dovrei prendere il peso molecolare in grammi/mole e da li ricavarmi il numero di atomi, e dato che per ipotesi abbiamo un elettrone libero per atomo la soluzione equivale al numero di atomi, è giusto?
1
voti
Si` signore. TI serve il peso atomico del rame, la densita` del rame e il numero di Avogadro.
E calcola anche l'effettiva velocita` dell'acqua nel tubo!
E calcola anche l'effettiva velocita` dell'acqua nel tubo!
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
1
voti
Temperatura ambiente: non cambia di molto per qualunque temperatura umana.
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
0
voti
Legenga: TT= pi greco
1l di acqua = 0,001 m cubi perciò 0,5 l/s = 0,0005 m cubi/s Sezione del tubo= TTr^2=0,0012 m^2 Velocità=0,0005/0,0012=0,42 m/s
Problema del rame
Allora considerando peso atomico= 63,546 uma densità=8920kg/m cubo e che una mole è uguale a 6,022x10^23
abbiamo che il volume molare=Peso atomico/densità=7,12x10^-3 m cubo/mol
1m cubo = 140,45 mol e perciò avremo 140,45 elettroni libero in un metro cubo di rame
1l di acqua = 0,001 m cubi perciò 0,5 l/s = 0,0005 m cubi/s Sezione del tubo= TTr^2=0,0012 m^2 Velocità=0,0005/0,0012=0,42 m/s
Problema del rame
Allora considerando peso atomico= 63,546 uma densità=8920kg/m cubo e che una mole è uguale a 6,022x10^23
abbiamo che il volume molare=Peso atomico/densità=7,12x10^-3 m cubo/mol
1m cubo = 140,45 mol e perciò avremo 140,45 elettroni libero in un metro cubo di rame
2
voti
Acqua: quasi giusto. La misura del tubo che avevo dato era diametro di 2cm, mentre tu hai preso raggio di 2cm e quindi hai trovato una velocita` 4 volte piu` lenta di quella effettiva. Comunque va bene.
Se vuoi scrivere le formule per bene, usa il comando tex che trovi in alto, sopra la finestra dove scrivi il messaggio. Per scrivere pigreca scrivi \pi, per r^2 scrivi r^2 e ottieni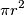 . Se vedi in giro una formula che ti piace, passale il mouse sopra e vedi come e` stata scritta in linguaggio latex.
. Se vedi in giro una formula che ti piace, passale il mouse sopra e vedi come e` stata scritta in linguaggio latex.
Altra osservazione e` sulle approssimazioni che hai fatto. VIsto che probabilmente fai i conti con la calcolatrice, usane le memorie per tenere i risultati intermedi, o le parentesi (o lo stack se e` una RPN) cosi` a ogni passaggio non introduci errori di troncamento: il risultato che hai trovato e` di circa il 5.6% maggiore del risultato "giusto".
Nel calcolo del numero di elettroni ci sono due errori: il peso atomico e` dato in grammi a mole e quando lo dividi per la densita` data in kilogrammi al metro cubo, ti scappa un fattore 1000.
Quello che ottieni dopo aver messo a posto i grammi e kilogrammi e` il numero di moli in un metrocubo, poi dobbiamo trovare il numero di atomi, quindi...
Se vuoi scrivere le formule per bene, usa il comando tex che trovi in alto, sopra la finestra dove scrivi il messaggio. Per scrivere pigreca scrivi \pi, per r^2 scrivi r^2 e ottieni
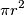 . Se vedi in giro una formula che ti piace, passale il mouse sopra e vedi come e` stata scritta in linguaggio latex.
. Se vedi in giro una formula che ti piace, passale il mouse sopra e vedi come e` stata scritta in linguaggio latex.Altra osservazione e` sulle approssimazioni che hai fatto. VIsto che probabilmente fai i conti con la calcolatrice, usane le memorie per tenere i risultati intermedi, o le parentesi (o lo stack se e` una RPN) cosi` a ogni passaggio non introduci errori di troncamento: il risultato che hai trovato e` di circa il 5.6% maggiore del risultato "giusto".
Nel calcolo del numero di elettroni ci sono due errori: il peso atomico e` dato in grammi a mole e quando lo dividi per la densita` data in kilogrammi al metro cubo, ti scappa un fattore 1000.
Quello che ottieni dopo aver messo a posto i grammi e kilogrammi e` il numero di moli in un metrocubo, poi dobbiamo trovare il numero di atomi, quindi...
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
1
voti
Mi spieghi meglio per quanto riguarda la calcolatrice? perché non so niente a riguardo e sarebbe ora che imparassi ad usarla correttamente, a partire dalle sigle in alto(es: DEG, RAD ecc ecc). Se è troppo da scrivere potresti consigliarmi un sito che spiega tutto in modo approfondito?
0
voti
 P.s. A proposito di calcolatrici,Isidoro predilige... il regolo calcolatore
P.s. A proposito di calcolatrici,Isidoro predilige... il regolo calcolatore "Non farei mai parte di un club che accettasse la mia iscrizione" (G. Marx)
-

 claudiocedrone
claudiocedrone
21,3k 4 7 9 - Master EY

- Messaggi: 15302
- Iscritto il: 18 gen 2012, 13:36
Chi c’è in linea
Visitano il forum: Nessuno e 55 ospiti

 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra)


