Es.di termodinamica: processo adiabatico
Moderatori: ![]() paolo a m,
paolo a m, ![]() DarioDT,
DarioDT, ![]() Guerra
Guerra
33 messaggi
• Pagina 2 di 4 • 1, 2, 3, 4
0
voti
sì, succede proprio questo.
-

 PietroBaima
PietroBaima
90,7k 7 12 13 - G.Master EY

- Messaggi: 12206
- Iscritto il: 12 ago 2012, 1:20
- Località: Londra
0
voti
se non sono in equilibrio non si può definire una temperatura o una pressione per il gas.
Inoltre, non è specificata la temperatura iniziale della seconda bombola. la seconda temperatura è più alta di quella iniziale. Come è possibile, se la trasformazione è un'espansione adiabatica?
Inoltre, non è specificata la temperatura iniziale della seconda bombola. la seconda temperatura è più alta di quella iniziale. Come è possibile, se la trasformazione è un'espansione adiabatica?
0
voti
musica94 ha scritto:se non sono in equilibrio non si può definire una temperatura o una pressione per il gas.
infatti non sono in condizioni stazionarie quando si apre la valvola, poi esaurito il transitorio ci arrivano.
inoltre l’andamento della temperatura e pressione del gas dipende dal tempo, con una cinetica di primo o secondo ordine in funzione dei poli del sistema fisico.
Avevo accennato vagamente a queste cose qui.
musica94 ha scritto:Inoltre, non è specificata la temperatura iniziale della seconda bombola.
ambiente?
musica94 ha scritto:la seconda temperatura è più alta di quella iniziale. Come è possibile, se la trasformazione è un'espansione adiabatica?
il gas si espande nella prima bombola quindi si raffredda, e non c’è scambio energetico con l’esterno, quindi...
-

 PietroBaima
PietroBaima
90,7k 7 12 13 - G.Master EY

- Messaggi: 12206
- Iscritto il: 12 ago 2012, 1:20
- Località: Londra
0
voti
Mi.piacerebbe vedere il procedimento
0
voti
Appena ho un attimo ci penso io. Adesso però ho da fare, scusate.
-

 PietroBaima
PietroBaima
90,7k 7 12 13 - G.Master EY

- Messaggi: 12206
- Iscritto il: 12 ago 2012, 1:20
- Località: Londra
0
voti
La risposta del libro sulla pressione finale è quella che, dal grande ammasso di ruggine che è il mio cervello, avrei indicato abbastanza facilmente...
Ma...leggendo il post 2 sembrerebbe sbagliata perché non è cp=cv...
Anche io non capisco la doppia temperatura, e trattandosi di esercizio "teorico" non mi interessa la temperatura della bombola vuota proprio perché...vuota!
Insomma non c'è gas al suo interno, e di solito non vengono considerate le pareti e la loro temperatura.
Darei per scontato, essendo adiabatica, che la T finale sia minore...quindi la prima delle due temp indicate e l'altra la considererei un refuso di stampa.
Aspetto di sapere anch'io cosa mi sfugge e cosa si porta a T più elevata di quella di partenza...
Ma...leggendo il post 2 sembrerebbe sbagliata perché non è cp=cv...
Anche io non capisco la doppia temperatura, e trattandosi di esercizio "teorico" non mi interessa la temperatura della bombola vuota proprio perché...vuota!
Insomma non c'è gas al suo interno, e di solito non vengono considerate le pareti e la loro temperatura.
Darei per scontato, essendo adiabatica, che la T finale sia minore...quindi la prima delle due temp indicate e l'altra la considererei un refuso di stampa.
Aspetto di sapere anch'io cosa mi sfugge e cosa si porta a T più elevata di quella di partenza...
0
voti
richiurci ha scritto:Insomma non c'è gas al suo interno, e di solito non vengono considerate le pareti e la loro temperatura.
Eh?

L'esercizio dice che alla fine nelle due bombole c'è la stessa pressione. Se non c'è gas all'interno dell'una, la sua pressione è zero, da cui consegue che anche nella seconda bombola la pressione è zero e che quindi non c'è gas. Insomma... abbiamo annichilito tutto?
Boiler
0
voti
La mia interpretazione del problema (che evidentemente va verificata da un'istanza superiore) è che avendo inizialmente il vuoto nella seconda bombola, il lavoro di espansione è nullo.
Inoltre visto che il processo è adiabatico non c'è scambio di calore con l'ambiente. La quantità di calore alla fine del processo deve quindi essere la stessa che si aveva all'inizio.
Sarà la distribuzione della quantità di calore tra le due bombole ad essere diversa.
La quantità di calore nelle due bombole (che indico con 1 e 2) alla fine (f= finale, i=iniziale) del processo sarà:
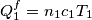
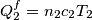
La quantità di gas in equiblibrio la ottieni con
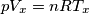
p è pari in ambedue i contenitori.
Inoltre vale che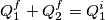
Come trovare p? Se lasciamo ai due gas tempo di raggiungere l'equlibrio termico (tra di loro, le bombole continuano ad essere perfettamente isolate) avremo che in ambo i contenitori pressione e temperatura sono pari. Il volume totale è conosciuto così come la quantità di materia (ce si spera non cambiare nel corso del processo ). Vale quindi nuovamente
). Vale quindi nuovamente  .
.
Se metti tutto assieme (occhio all'uso della giusta versione di c) dovresti ottenere un sistema di equazioni risolvibile.
Boiler
Inoltre visto che il processo è adiabatico non c'è scambio di calore con l'ambiente. La quantità di calore alla fine del processo deve quindi essere la stessa che si aveva all'inizio.
Sarà la distribuzione della quantità di calore tra le due bombole ad essere diversa.
La quantità di calore nelle due bombole (che indico con 1 e 2) alla fine (f= finale, i=iniziale) del processo sarà:
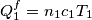
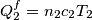
La quantità di gas in equiblibrio la ottieni con
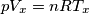
p è pari in ambedue i contenitori.
Inoltre vale che
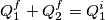
Come trovare p? Se lasciamo ai due gas tempo di raggiungere l'equlibrio termico (tra di loro, le bombole continuano ad essere perfettamente isolate) avremo che in ambo i contenitori pressione e temperatura sono pari. Il volume totale è conosciuto così come la quantità di materia (ce si spera non cambiare nel corso del processo
 .
.Se metti tutto assieme (occhio all'uso della giusta versione di c) dovresti ottenere un sistema di equazioni risolvibile.
Boiler
33 messaggi
• Pagina 2 di 4 • 1, 2, 3, 4
Torna a Termotecnica, illuminotecnica, acustica
Chi c’è in linea
Visitano il forum: Nessuno e 25 ospiti

 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra) pigreco]=π
pigreco]=π



