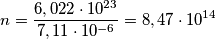1l di acqua = 0,001 m cubi perciò 0,5 l/s = 0,0005 m cubi/s Sezione del tubo= \pi r^2=0,00031 m quadrati Velocità=0,0005/0,00031=1,591549432 m/s
Peso atomico= 63,546 g/mol =0,063546 kg/mol Densità=8920 kg/m cubi Vm= 0,063546/8920= 7,12*10^-6 m cubi/mol Siccome 1mol=6,022*10^23 allora Atomi in un m cubo di Cu=(6,022*10^23)*7,12*10^-6=42900,67399
PS: non ho approssimato così puoi capire se il calcolo è venuto giusto, perché ho usato le memorie interne.
[user]IsodoroKZ[/user]
Deriva degli elettroni
Moderatori: ![]() carloc,
carloc, ![]() g.schgor,
g.schgor, ![]() BrunoValente,
BrunoValente, ![]() IsidoroKZ
IsidoroKZ
4
voti
Cristhian ha scritto:1l di acqua = 0,001 m cubi perciò 0,5 l/s = 0,0005 m cubi/s Sezione del tubo= \pi r^2=0,00031 m quadrati Velocità=0,0005/0,00031=1,591549432 m/s
Ok adesso va bene. Usa le memorie interne, pero` alla fine, ma solo alla fine, non mettere troppe cifre. Quando dico che la portata e` di 0.5 l/con che accuratezza conosco il dato? E il diametro di 2cm quanto bene lo conosco? Tutto cio` per dire che se va bene si puo` dire 1.59 m/s e forse credere al 9 finale e` eccessivo. Il problema dell'errore di misura e` di quelli complicati. Per il momento vai piu` o meno a buon senso, 3 cifre significative di solito vanno bene.
Cristhian ha scritto:Peso atomico= 63,546 g/mol =0,063546 kg/mol Densità=8920 kg/m cubi Vm= 0,063546/8920= 7,12*10^-6 m cubi/mol Siccome 1mol=6,022*10^23 allora Atomi in un m cubo di Cu=(6,022*10^23)*7,12*10^-6=42900,67399
Mi pare ci siano due cose che non vanno. Il numero di atomi al metro cubo e` dato da numero di atomi per mole (numero di Avogadro
 ) per il numero di moli al metrocubo.
) per il numero di moli al metrocubo.Quello che hai calcolato e` il volume molare:
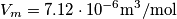 . Per trovare il numero di atomi per unita` di volume secondo me devi calcolare
. Per trovare il numero di atomi per unita` di volume secondo me devi calcolare 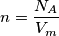
Se fai l'analisi delle unita` di misura vedi che il numero di Avogadro e` misurato in
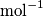 , il volume molare e` misurato in
, il volume molare e` misurato in  vedi che l'espressione che hai usato non da` un metricubi al denominatore.
vedi che l'espressione che hai usato non da` un metricubi al denominatore.Poi c'e` un secondo problema. Guardiamo solo i numeri: moltiplichi
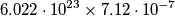 . Prima di fare i conti devi dare una stima che e` circa cosi`
. Prima di fare i conti devi dare una stima che e` circa cosi`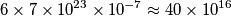 . Il risultato e`solo una approssimazione, ma da` una idea del risultato che devi aspettarti: di sicuro non 429000 o giu` di li`.
. Il risultato e`solo una approssimazione, ma da` una idea del risultato che devi aspettarti: di sicuro non 429000 o giu` di li`.Nota che questa risposta e` complicata perche' coinvolge i conti approssimati, la stima dell'errore... Ma sono tutte cose che servono.
Calcola poi la densita` di carica libera per unita` di volume (in pratica i coulomb al metrocubo) del rame. E poi ci siamo quasi per calcolare la velocita` di deriva degli elettroni.
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
0
voti
Non ti preoccupare di rispondere in modo lungo o complicato, è proprio quello che cerco, comunque per il problema del rame l'ho svolto nuovamente utilizzando il seguente metodo:
prima mi sono calcolato la massa di un metro cubo di rame che essendo cioè
cioè 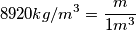 ovviamente
ovviamente 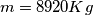
numero di moli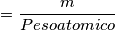 trovato il numero di moli lo moltiplico per
trovato il numero di moli lo moltiplico per 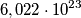 (atomi in una mole) e ho trovato il numero di atomi che è uguale al numero di elettroni liberi. Spero sia giusto, se lo è farò i dovuti calcoli ovviamente.
(atomi in una mole) e ho trovato il numero di atomi che è uguale al numero di elettroni liberi. Spero sia giusto, se lo è farò i dovuti calcoli ovviamente.
prima mi sono calcolato la massa di un metro cubo di rame che essendo
 cioè
cioè 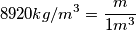 ovviamente
ovviamente 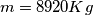
numero di moli
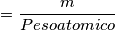 trovato il numero di moli lo moltiplico per
trovato il numero di moli lo moltiplico per 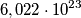 (atomi in una mole) e ho trovato il numero di atomi che è uguale al numero di elettroni liberi. Spero sia giusto, se lo è farò i dovuti calcoli ovviamente.
(atomi in una mole) e ho trovato il numero di atomi che è uguale al numero di elettroni liberi. Spero sia giusto, se lo è farò i dovuti calcoli ovviamente.1
voti
Se vuoi farlo cosi`, va bene. Il kilogrammo ha il simbolo con la k minuscola.
Quando hai trovato il numero di atomi, e quindi il numero di elettroni, moltiplica per la carica dell'elettrone e hai la carica disponibile per la conduzione in un metro cubo di rame.
Quando hai trovato il numero di atomi, e quindi il numero di elettroni, moltiplica per la carica dell'elettrone e hai la carica disponibile per la conduzione in un metro cubo di rame.
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
1
voti
SI puo` anche fare come avevamo gia` detto nel messaggio 32, come rapporto fra numero di Avogadro e volume molare.
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
0
voti
Ma la spiegazione della formula  la posso trovare su google? Se sì come la cerco? perché se come formula è più corretta ed inerente al percorso che mi stai facendo fare voglio capirla e usare quella.
la posso trovare su google? Se sì come la cerco? perché se come formula è più corretta ed inerente al percorso che mi stai facendo fare voglio capirla e usare quella.
 la posso trovare su google? Se sì come la cerco? perché se come formula è più corretta ed inerente al percorso che mi stai facendo fare voglio capirla e usare quella.
la posso trovare su google? Se sì come la cerco? perché se come formula è più corretta ed inerente al percorso che mi stai facendo fare voglio capirla e usare quella.2
voti
Non e` detto che sia il modo piu` giusto, semplicemente mi sembra piu` elegante.
La formula e` facile: se una mole ha un volume di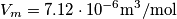 quante moli ci sono in un metrocubo? Il reciproco di Vm da` le moli al metro cubo
quante moli ci sono in un metrocubo? Il reciproco di Vm da` le moli al metro cubo 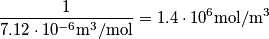 .
.
Il Vm a denominatore e` in pratica solo il numero di moli per unita` di volume. Poi se moltiplichi questo per il numero di Avogadro...
La formula e` facile: se una mole ha un volume di
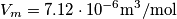 quante moli ci sono in un metrocubo? Il reciproco di Vm da` le moli al metro cubo
quante moli ci sono in un metrocubo? Il reciproco di Vm da` le moli al metro cubo 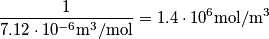 .
.Il Vm a denominatore e` in pratica solo il numero di moli per unita` di volume. Poi se moltiplichi questo per il numero di Avogadro...
Per usare proficuamente un simulatore, bisogna sapere molta più elettronica di lui
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
Plug it in - it works better!
Il 555 sta all'elettronica come Arduino all'informatica! (entrambi loro malgrado)
Se volete risposte rispondete a tutte le mie domande
0
voti
Ah ecco!! okok ora ho capito e mi sembra giusto utilizzare la formula  poiché siamo essere intelligenti e scegliere le vie più semplici e brevi è una delle cose che ci distingue dagli animali.
poiché siamo essere intelligenti e scegliere le vie più semplici e brevi è una delle cose che ci distingue dagli animali.
 poiché siamo essere intelligenti e scegliere le vie più semplici e brevi è una delle cose che ci distingue dagli animali.
poiché siamo essere intelligenti e scegliere le vie più semplici e brevi è una delle cose che ci distingue dagli animali.Chi c’è in linea
Visitano il forum: Google [Bot], Google Adsense [Bot] e 38 ospiti

 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra)