xeletro91 ha scritto:Il tuo modello



magari!



xeletro91 ha scritto:Ogni processo spontaneo tende a portarsi a configurazioni a minor energia potenziale, quindi quest'ultima all'equilibrio sarà per forza di cose diminuita.
In termodinamica non esiste un solo tipo di energia potenziale; quando temperatura e pressione sono costanti il potenziale termodinamico è rappresentato dall'energia libera di Gibbs. Ed' effettivamente essa è minima all'equilibrio!
Ora provo a spiegarlo da un'altra prospettiva...
Prendiamo la sezione di un cristallo tipo NaCl, a temperatura e pressione ambiente. Al tempo

il cristallo è perfetto, alla stessa temperatura dell'ambiente. (I cerchietti blu sotto le particelle rappresentano la loro energia cinetica).
L'energia cinetica dovuta agli urti delle particelle vibranti attorno alla loro posizione, o delle particelle d'aria che urtano le paretti esterne del cristallo, si converte in energia potenziale; formando il difetto e diminuendo la temperatura del corpo.
Essendo ora il corpo, più freddo dell'ambiente esso ne assorbirà il calore, portandosi alla stessa temperatura. Dal punto di vista particellare, gli urti delle molecole d'aria fanno aumentare l'energia cinetica delle particelle cristalline, ristabilendola (

).
Questo processo continua pertanto che il potenziale termodinamico non è minimo.
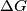
è il potenziale termodinamico,

è l'energia necessaria alla formazione del difetto,
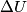
è l'incremento di energia interna dovuta a un difetto, coincide con l'entalpia di formazione.
Secondo me è meglio spiegare il fenomeno assumendo l'aumento di entropia come assioma. E sviluppare la teoria di conseguenza. Anche perché questo è il secondo principio della termodinamica.
cronos80 ha scritto:non è assolutamente detto che questo calore non innalzi la temperatura dell'oggetto, causandone una variazione di entalpia.
xeletro91 ha scritto:Il processo è endotermico a T e P= costante
Non ha mica detto:
Il processo è endotermico quindi T e P = costante



Dante.
xeletro91, ma perché affermi che essendo il processo endotermico la temperatura è costante?


 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra)

 il cristallo è perfetto, alla stessa temperatura dell'ambiente. (I cerchietti blu sotto le particelle rappresentano la loro energia cinetica).
il cristallo è perfetto, alla stessa temperatura dell'ambiente. (I cerchietti blu sotto le particelle rappresentano la loro energia cinetica).

 ).
).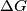 è il potenziale termodinamico,
è il potenziale termodinamico, è l'energia necessaria alla formazione del difetto,
è l'energia necessaria alla formazione del difetto,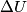 è l'incremento di energia interna dovuta a un difetto, coincide con l'entalpia di formazione.
è l'incremento di energia interna dovuta a un difetto, coincide con l'entalpia di formazione.

 pigreco]=π
pigreco]=π
