ad ogni modo ecco il mio primo tentativo :
1)qui ho utilizzato il cp preso da wikipedia
Ho calcolato la massa molecolare
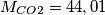
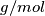
poi da questa ho calcolato la massa in
 :
: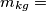
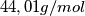
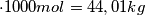
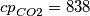
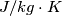
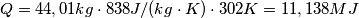
il risultato previsto dal libro è:
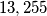
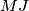
Moderatori: ![]() paolo a m,
paolo a m, ![]() DarioDT,
DarioDT, ![]() Guerra
Guerra
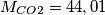
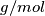
 :
: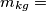
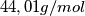
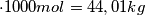
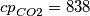
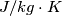
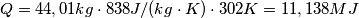
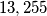
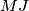
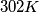 ho fatto esattamente come scritto per il cp dell'acqua nella didascalia della tabella 3 pagina 43 (ciò che non capisco è come mai nella tabella vengono riportati i coefficienti come per esempio
ho fatto esattamente come scritto per il cp dell'acqua nella didascalia della tabella 3 pagina 43 (ciò che non capisco è come mai nella tabella vengono riportati i coefficienti come per esempio 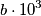 se poi nella formula compare
se poi nella formula compare 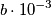 ? )
? )
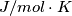
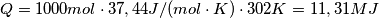
musica94 ha scritto:ad ogni modo ecco il mio primo tentativo :
musica94 ha scritto:1)qui ho utilizzato il cp preso da wikipedia
Ho calcolato la massa molecolare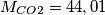
poi da questa ho calcolato la massa in:
musica94 ha scritto: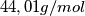
musica94 ha scritto: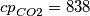
il risultato previsto dal libro è: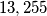


![cp^{*}=a+b \cdot T +c \cdot T^{2}+d \cdot T^{3}+e \cdot T^{-2}
[J\cdot {mol^{-1}} \cdot{K^{-1}}]
T in [K] cp^{*}=a+b \cdot T +c \cdot T^{2}+d \cdot T^{3}+e \cdot T^{-2}
[J\cdot {mol^{-1}} \cdot{K^{-1}}]
T in [K]](/forum/latexrender/pictures/fddeb14f76d6f7cf241ccc05d918aa4f.png)
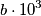 se poi nella formula compare
se poi nella formula compare 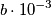 ? (riferendomi al calcolo del cp dell'acqua fatto nella didascalia sottostante la tabella 3 a pagina 43)
? (riferendomi al calcolo del cp dell'acqua fatto nella didascalia sottostante la tabella 3 a pagina 43)
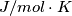
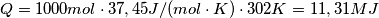
musica94 ha scritto:qualche consiglio?


musica94 ha scritto: ciò che non capisco è come mai nella tabella vengono riportati i coefficienti come per esempiose poi nella formula compare
? (riferendomi al calcolo del cp dell'acqua fatto nella didascalia sottostante la tabella 3 a pagina 43)
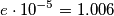
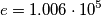


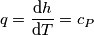
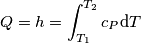
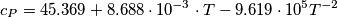


PietroBaima ha scritto:musica94 ha scritto:qualche consiglio?
Ti sembra che da 298 K a 600 K la variazione di T sia piccola? (prima di passare al secondo problema, finiamo il primo)
PietroBaima ha scritto:musica94 ha scritto: ciò che non capisco è come mai nella tabella vengono riportati i coefficienti come per esempiose poi nella formula compare
? (riferendomi al calcolo del cp dell'acqua fatto nella didascalia sottostante la tabella 3 a pagina 43)
Torna a Termotecnica, illuminotecnica, acustica
Visitano il forum: Nessuno e 58 ospiti