stefanopc ha scritto:Il cloruro ferrico non è pericoloso per la pelle come un vero acido.
Dipende dalla concentrazione. Le macchie che lascia sulla pelle portano del cloro in circolo e questo non è un bene per tutta una serie di ragioni, inoltre è molto velenoso se ingerito (anche se per fortuna non conosco nessuno che se lo sia bevuto).
Per tutti: per favore fatela finita una volta per tutte di chiamare acido il percloruro ferrico, che invece è un sale. E' irritante sentire chiamare acido un sale su di un forum tecnico (seppur non specializzato in chimica).
boiler ha scritto:La velocità dipende dalla concentrazione dei reagenti. Se puoi procurarti l'acqua ossigenata al 30% (che però è pericolosa!) è estremamente rapido, controllabile e pulito.
Aggiungo di non versare mai l'acqua ossigenata nell'acido, ma far gocciolare l'acido nell'acqua ossigenata.
Questo è molto importante, come anche usare occhiali da chimico quando lo si fa.
boiler ha scritto:Usando acido muriatico (=cloridrico) si forma cloruro di rame, che è solubile in acqua e quindi "sparisce" e non disturba.
Si ha però formazione di cloro gassoso, quindi conviene farlo all'aperto.
L'acido cloridrico reagisce con l'acqua ossigenata formando cloro gassoso e acqua.
Il cloro formato e l'acqua ossigenata ossidano il rame metallico (Cu) trasformandolo in cloruro di rame (II) (CuCl₂).
Finché è poco il cloruro di rame non disturba, poi il rame metallico forma una soluzione verde-azzurra di cloruro di rame (II) e quando la soluzione satura precipita.
boiler ha scritto:Usando acido citrico ti ritrovi con citrato di rame, che precipita e quindi intralcia.
Non subito, anche qui deve arrivare a soluzione e la reazione è lenta.
Però (penso, non sono sicuro) che un acido complesso come il citrico possa formare dei sali complessi di rame e quelli fanno casino.
boiler ha scritto:Forse usando alcido ammidosolfonico (contenuto in molti prodotti anticalcare) ottieni un sale solubile (non sono sicuro!)
Qui purtroppo sono costretto a contraddirti, l'acido ammidosolfonico (H₃NSO₃) o acido solfammico, è un acido forte che, in condizioni normali, non reagisce col rame da solo perché non ha forti proprietà ossidanti.
Serve anche qui un agente ossidante, tipo l'acqua ossigenata.
Credo sia possibile che in condizioni particolari (come alte temperature o concentrazioni estremamente elevate) possa esserci qualche interazione, ma in generale, per usi pratici qui esposti non reagisce affatto.
Pietro

 Elettrotecnica e non solo (admin)
Elettrotecnica e non solo (admin) Un gatto tra gli elettroni (IsidoroKZ)
Un gatto tra gli elettroni (IsidoroKZ) Esperienza e simulazioni (g.schgor)
Esperienza e simulazioni (g.schgor) Moleskine di un idraulico (RenzoDF)
Moleskine di un idraulico (RenzoDF) Il Blog di ElectroYou (webmaster)
Il Blog di ElectroYou (webmaster) Idee microcontrollate (TardoFreak)
Idee microcontrollate (TardoFreak) PICcoli grandi PICMicro (Paolino)
PICcoli grandi PICMicro (Paolino) Il blog elettrico di carloc (carloc)
Il blog elettrico di carloc (carloc) DirtEYblooog (dirtydeeds)
DirtEYblooog (dirtydeeds) Di tutto... un po' (jordan20)
Di tutto... un po' (jordan20) AK47 (lillo)
AK47 (lillo) Esperienze elettroniche (marco438)
Esperienze elettroniche (marco438) Telecomunicazioni musicali (clavicordo)
Telecomunicazioni musicali (clavicordo) Automazione ed Elettronica (gustavo)
Automazione ed Elettronica (gustavo) Direttive per la sicurezza (ErnestoCappelletti)
Direttive per la sicurezza (ErnestoCappelletti) EYnfo dall'Alaska (mir)
EYnfo dall'Alaska (mir) Apriamo il quadro! (attilio)
Apriamo il quadro! (attilio) H7-25 (asdf)
H7-25 (asdf) Passione Elettrica (massimob)
Passione Elettrica (massimob) Elettroni a spasso (guidob)
Elettroni a spasso (guidob) Bloguerra (guerra)
Bloguerra (guerra)


 pigreco]=π
pigreco]=π




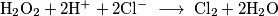


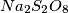 e scrivilo bene! Diamine!
e scrivilo bene! Diamine!